
In ons maagdarmkanaal zitten tal van micro-organismen. Denk aan bacteriën, virussen en schimmels. Samen vormen die de darmmicrobiota, het microbioom of de darmflora. De activiteit en samenstelling daarvan kan een effect hebben op onze gezondheid. Om een goede darmgezondheid te bewaren zijn prebiotica en probiotica essentieel. Die twee termen worden veelal door elkaar gebruikt, maar betekenen wel degelijk iets anders. Wat is het verschil? Wat is hun functie en welke gezondheidsvoordelen hebben ze? Het antwoord vind je hier.
De definitie van probiotica
De laatste decennia is al heel wat onderzoek gedaan naar de gezondheidsvoordelen van probiotica. Probiotica is afgeleid van het Grieks waarbij Pro ‘voor’ en Biotica ‘leven’ betekent (1). De meest recente definitie van probiotica die de FDA en WHO gezamenlijk hebben opgesteld is de volgende: (probiotica) zijn micro-organismen die, wanneer zij in voldoende mate worden toegediend, een gezondheidsvoordeel opleveren voor het menselijk lichaam. Probiotica bevatten dus levende bacteriën (2).Wist je trouwens dat de bacteriële kolonisatie van het maagdarmkanaal al begint tijdens de geboorte, wanneer het pasgeboren kind in contact komt met de baarmoederhals- en vaginale flora van de moeder? Vandaar dat men ook een verschil ziet in de samenstelling van het microbioom bij baby’s die geboren zijn met keizersnede en kinderen die via de vaginale weg zijn geboren. Bij een geboorte via keizersnede loopt een baby deze eerste kolonisatie dus mis. Voor meer info verwijzen we je graag door naar de recente studie van Long G., et al (2021) (3).
Wat is het nut van probiotica?
De term probiotica werd voor het eerst geïntroduceerd door Vergin, toen hij de schadelijke effecten van antibiotica en andere microbiële stoffen op de microbiële darmpopulatie bestudeerde. Hij merkte op dat probiotica gunstig waren voor de microflora in de darmen (1). Darmbacteriën spelen een cruciale rol bij het in stand houden van de immuun- en metabolische homeostase en de bescherming tegen ziekteverwekkers. Een veranderde samenstelling van de darmbacteriën (dysbiose) is al in verband gebracht met ontstekingsziekten en infecties. Kortom probiotische bacteriën kunnen verschillende gezondheidsvoordelen bieden door het normaliseren van een verstoord microbioom, het uitsluiten van pathogenen, en het verhogen van de productie van SCFA (4-6). SCFA staat voor Short-Chain Fatty Acids ofwel korte keten vetzuren zoals acetaat, propionaat, en butyraat (boterzuur). Meer hierover lees je verderop in het stukje over prebiotica.
Voornamelijk de Lactobacillus en Bifidobacterium zijn gerapporteerd als gunstige probiotische bacteriestammen. De representatieve soorten zijn onder meer L. acidophilus, L. casei, L. plantarum, B. lactis, B. longum, en B. bifidum (7). Probiotica worden gemeten in kolonievormende eenheden (CFU). Die geven het aantal levensvatbare cellen aan. Hoeveelheden kunnen op productetiketten worden aangegeven als bijvoorbeeld 1 x 109 voor 1 miljard CFU of 1 x 1010 voor 10 miljard CFU. Veel probiotische supplementen bevatten 1 tot 10 miljard CFU per dosis, maar sommige producten bevatten tot 50 miljard CFU of meer. Een hoger aantal CFU's verbetert echter niet noodzakelijkerwijs de gezondheidseffecten van het product (8).
Ben je op zoek naar een probioticum? Dan hebben wij Debaflor in het gamma, een probioticum ter ondersteuning van de darmflora, spijsvertering en immuniteit.
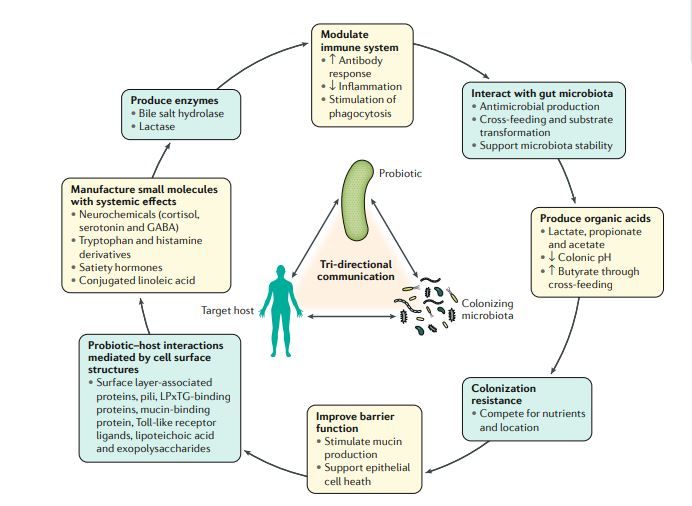
Probiotica zijn geen prebiotica (en omgekeerd)
Probiotica mogen niet worden verward met prebiotica. Dat zijn meestal complexe koolhydraten (zoals inuline en andere fructo-oligosacchariden) die door micro-organismen in het maagdarmkanaal worden gebruikt als stofwisselingsbrandstof (9). In sommige klinische studies wordt een probioticum toegediend in combinatie met prebiotica om de goede bacteriegroei te bevorderen. De combinatie wordt ook wel een synbioticum genoemd. Prebiotica moet je eigenlijk zien als de voeding voor de darmbacteriën terwijl probiotica de bacteriën zelf zijn.
Wat zijn prebiotica en wat is hun effect?
De vereisten van een prebioticum zijn dat ze in het bovenste deel van het maagdarmkanaal kunnen worden gefermenteerd door de intestinale microbiota. Ze stimuleren selectief de groei en diversiteit van nuttige bacteriën en hebben een positief effect op de gezondheid van de gastheer. Van prebiotica zoals galacto-oligosacchariden (GOS) en fructo-oligosacchariden (FOS) is aangetoond dat ze het microbioom verbeteren door de toename van bifidobacteriën en afname van E. coli (10). Verschillende verbindingen zijn getest om hun functie als prebiotica te bepalen. FOS, GOS en trans-galacto-oligosacchariden (TOS) zijn de meest voorkomende prebiotica.
Fermentatie van prebiotica door de darmmicrobiota produceert vetzuren met een korte keten (SCFA's) zoals melkzuur, boterzuur en propionzuur. Dit zijn eindproducten van bacteriële fermentatie van met name onverteerbare koolhydraten in de dikke darm (9). Deze producten kunnen meerdere effecten hebben op het lichaam. Zo beïnvloedt propionaat bijvoorbeeld T helper 2 in de luchtwegen en macrofagen, evenals dendritische cellen in het beenmerg (11, 12). Een afname van het aantal bacteriën dat metabolieten zoals SCFA’s produceert wordt vaak als oorzaak aangewezen bij patiënten met inflammatoire darmziekten (IBD), prikkelbaar darmsyndroom (IBS), diabetes type 2 (T2D), obesitas, bacteriële infecties, auto-immuunziekten of kankerpatiënten (13). Zo kan het doeltreffend zijn bij het prikkelbare darmsyndroom en de ziekte van crohn (14). Er is ook vastgesteld dat de consumptie van prebiotica het risico op het ontstaan van allergische huidziekten zoals atopische dermatitis vermindert, ook bij zuigelingen (15, 16). Het prebioticum FOS vermindert tevens de expressie van IL-6 (17). Inteleukine 6 is een cytokine dat een belangrijke rol speelt bij chronische ontstekingsziekten.
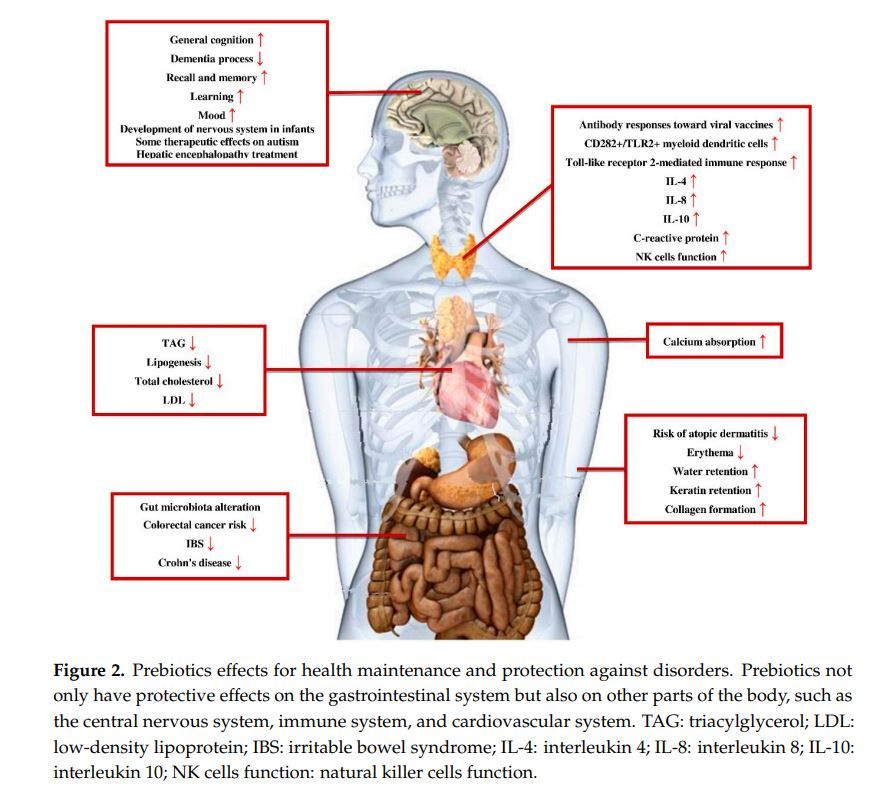
Wat zijn prebiotische voedingsmiddelen?
Prebiotica komen van nature voor in verschillende levensmiddelen zoals asperges, knoflook, cichorei, uien, aardperen, tarwe, honing, banaan, gerst, tomaat, rogge, soja, erwten, bonen, zeewieren en microalgen. Vanwege hun lage concentratie in levensmiddelen worden ze op grote industriële schaal geproduceerd onder de vorm van FOS en GOS (18). Zoals gezegd zijn de producten van de afbraak van prebiotica voornamelijk SCFA’s. Deze moleculen kunnen door de darmwand opgenomen worden en in de bloedcirculatie terechtkomen. Daarom zijn prebiotica niet enkel in staat om het maagdarmkanaal te beïnvloeden maar ook andere organen en systemen (19).
Er wordt algemeen aangenomen dat prebiotica geen ernstige bijwerkingen hebben. Ze worden naar de dikke darm getransporteerd om gefermenteerd te worden door de darmmicrobiota. Hoeveel prebiotica heb je nodig? Een dagelijkse dosis van 2,5-10 g prebiotica volstaat.
Ben je op zoek naar een prebioticum? Dan hebben wij met Deba Pharma FOS in het gamma.
Tot slot nog dit: wist je dat antibiotica, maagzuurremers en antipsychotica een invloed hebben op het microbioom?
- Antibiotica:
Zijn een veel voorkomende oorzaak van acute diarree. Antibioticabehandeling verstoort immers vaak het darmmicrobioom en kan, door vermindering van de microbiële diversiteit, leiden tot een verlies van microbieel metabolisme (met als gevolg osmotische diarree door overmatig vocht in de darm), verlies van kolonisatieresistentie (met als gevolg meer infecties door andere pathogenen), en verhoogde darmmotiliteit (21). Tot 30 procent van de patiënten die antibiotica gebruiken, krijgt te maken met antibiotica-geassocieerde diarree (AAD) (22). Van de probiotische stammen Lactobacillus rhamnosus GG als Saccharomyces boulardii is aangetoond dat ze het risico op AAD verminderen (23). Inname van probiotica binnen 2 dagen na de eerste antibioticadosis is effectiever dan te beginnen op een later moment.
- Maagzuurremers:
Ook wel protonpompremmers (PPI’s) zijn een veelgebruikte klasse van geneesmiddelen die de pH in de maag verhogen. PPI’s worden gebruikt bij gastro-oesofageale reflux, maagzweren en H. pylori-infectie. Veel chronisch zieke patiënten gebruiken langdurig PPI’s. Meta-analyses hebben aangetoond dat PPI-gebruik het risico op het ontwikkelen van SIBO verhoogt (Small Intestinal Bacterial Overgrowth) (24). Een SIBO kan leiden tot obstipatie, diarree, buikpijn, buikkrampen, gasvorming, ...
- naast antibiotica een maagzuurremers kunnen ook antipsychotica een negatieve invloed hebben op de microbiële diversiteit (25,26).
Conclusie? Draag zorg voor je darmen want ze hebben een brede functie voor je algemene gezondheid. Hou je goed!
1. J Food Sci Technol (December 2015) 52(12):7577–7587
2. Markowiak, P.; Slizewska, K. Effects of probiotics, prebiotics, and synbiotics on human health. Nutrients 2017, 9, 1021.
3. Long G, Hu Y, Tao E, et al. The Influence of Cesarean Section on the Composition and Development of Gut Microbiota During the First 3 Months of Life. Front Microbiol. 2021;12:691312. Published 2021 Aug 18. doi:10.3389/fmicb.2021.691312
4. Dimidi, E.; Christodoulides, S.; Scott, S.M.; Whelan, K. Mechanisms of action of probiotics and the gastrointestinal microbiota on gut motility and constipation. Adv. Nutr. 2017, 8, 484–494
5. Plaza-Diaz, J.; Ruiz-Ojeda, F.J.; Gil-Campos, M.; Gil, A. Mechanisms of action of probiotics. Adv. Nutr. 2019, 10, S49–S66
6. LeBlanc, J.G.; Chain, F.; Martin, R.; Bermudez-Humaran, L.G.; Courau, S.; Langella, P. Beneficial effects on host energy metabolism of short-chain fatty acids and vitamins produced by commensal and probiotic bacteria. Microb. Cell Fact. 2017, 16, 79
7. Balakrishnan, Kunasundari, Beneficial Properties of Probiotics Early view, Tropical Life Sciences Research 2016
8. https://ods.od.nih.gov/factsheets/Probiotics-HealthProfessional/#disc
9. Hijova E, Chmelarova A. Short chain fatty acids and colonic health. Bratisl Lek Listy. 2007;108(8):354-8. PMID: 18203540.
10. Musilova, S.; Rada, V.; Marounek, M.; Nevoral, J.; Duskova, D.; Bunesova, V.; Vlkova, E.; Zelenka, R. Prebiotic effects of a novel combination of galactooligosaccharides and maltodextrins. J. Med. Food 2015, 18, 685–689
11. Stinson, L.F.; Payne, M.S.; Keelan, J.A. Planting the seed: Origins,
composition, and postnatal health significance of the fetal gastrointestinal
microbiota. Crit. Rev. Microbiol. 2017, 43, 352–369. [CrossRef] Foods 2019, 8,
92 18 of 27
12. Trompette, A.; Gollwitzer, E.S.; Yadava, K.; Sichelstiel, A.K.; Sprenger, N.; Ngom-Bru, C.; Blanchard, C.; Junt, T.; Nicod, L.P.; Harris, N.L.; et al. Gut microbiota metabolism of dietary fiber influences allergic airway disease and hematopoiesis. Nat. Med. 2014, 20, 159–166.
13. Markowiak-Kopeć P, Śliżewska K. The Effect of Probiotics on the Production of Short-Chain Fatty Acids by Human Intestinal Microbiome. Nutrients. 2020;12(4):1107. Published 2020 Apr 16. doi:10.3390/nu12041107
14. Silk, D.; Davis, A.; Vulevic, J.; Tzortzis, G.; Gibson, G. Clinical trial: The effects of a trans-galactooligosaccharide prebiotic on faecal microbiota and symptoms in irritable bowel syndrome. Aliment. Pharmacol. Ther. 2009, 29, 508–518.
15. Grüber, C.; van Stuijvenberg, M.; Mosca, F.; Moro, G.; Chirico, G.; Braegger, C.P.; Riedler, J.; Boehm, G.;Wahn, U.; MIPS 1 Working Group. Reduced occurrence of early atopic dermatitis because of immunoactive prebiotics among low-atopy-risk infants. J. Allergy Clin. Immunol. 2010, 126, 791–797.
16. Moro, G.; Arslanoglu, S.; Stahl, B.; Jelinek, J.;Wahn, U.; Boehm, G. A mixture of prebiotic oligosaccharides reduces the incidence of atopic dermatitis during the first six months of age. Arch. Dis. Childhood 2006, 91,814–819. [CrossRef] [PubMed] Foods 2019, 8, 92 24 of 27
17. Guigoz, Y.; Rochat, F.; Perruisseau-Carrier, G.; Rochat, I.; Schiffrin, E. Effects of oligosaccharide on the faecal flora and non-specific immune system in elderly people. Nutr. Res. 2002, 22, 13–25.
18. Al-Sheraji, S.; Ismail, A.; Manap, M.; Mustafa, S.; Yusof, R.; Hassan, F. Prebiotics as functional foods: A review. J. Funct Foods 2013, 5, 1542–1553
19. den Besten, G.; van Eunen, K.; Groen, A.K.; Venema, K.; Reijngoud, D.-J.; Bakker, B.M. The role of short-chain fatty acids in the interplay between diet, gut microbiota, and host energy metabolism. J. Lipid Res. 2013, 54, 2325–2340.
20. Ahn J, Hayes RB. Environmental Influences on the Human Microbiome and Implications for Noncommunicable Disease. Annu Rev Public Health. 2021;42:277-292. doi:10.1146/annurev-publhealth-012420-105020
21. Ki Cha B, Mun Jung S, Hwan Choi C, Song ID, Woong Lee H, Joon Kim H, et al. The effect of a multispecies probiotic mixture on the symptoms and fecal microbiota in diarrhea-dominant irritable bowel syndrome: a randomized, double-blind, placebo-controlled trial. J Clin Gastroenterol 2012;46:220-7. [PubMed abstract]
22. Silverman MA, Konnikova L, Gerber JS. Impact of antibiotics on necrotizing enterocolitis and antibiotic-associated diarrhea. Gastroenterol Clin North Am 2017;46:61-76. [PubMed abstract]
23. Szajewska H, Kolodziej M. Systematic review with meta-analysis:
Saccharomyces boulardii in the prevention of antibiotic-associated diarrhoea.
Aliment Pharmacol Ther 2015;42:793-801
24. Su, T.; Lai, S.; Lee, A.; He, X.; Chen, S. Meta-analysis: Proton
pump inhibitors moderately increase the risk of small intestinal bacterial
overgrowth. J. Gastroenterol. 2018, 53, 27–36.
25. O’Donoghue, C.; Solomon, K.; Fenelon, L.; Fitzpatrick, F.; Kyne, L. Effect of proton pump inhibitors and antibiotics on the gut microbiome of hospitalised older persons. J. Infect. 2016, 72, 498–500.
26. Zhang, L.; Huang, Y.; Zhou, Y.; Buckley, T.; Wang, H.H. Antibiotic administration routes significantly influence the levels of antibiotic resistance in gut microbiota. Antimicrob. Agents Chemother. 2013, 57, 3659–3666. [CrossRef] [PubMed]
Wat is het verschil tussen probiotica en prebiotica?